一.无信号
![]()
1.样本原因
①样本不表达或者表达较低
选择合适的样本,进行适当的刺激处理
②样本制备不当
添加蛋白酶抑制剂和磷酸酶抑制剂;注意制备样本的细节以及制备好之后的保存条件,防止蛋白降解;选择合适的细胞组分进行制样
③上样量太少
增加上样量,细胞推荐20-50ug,组织推荐50-100ug
抗体原因
①抗体选择不当
选择合适的抗体,包括种属,适用范围
②抗体保存不当
按照抗体说明书进行保存
③抗体孵育时间或浓度不足
延长抗体孵育时间,增加抗体孵育浓度
实验操作
①转膜不当
根据目的蛋白分子量选择合适的膜;优化转膜电压、电流以及时间,转膜后用丽春红或者考马斯染料确认转膜效率
②封闭过度
减少封闭液浓度,减少封闭时间;确保不含高于0.1%的叠氮化钠
③显示剂失效
更换可正常使用的显色剂
二.高背景多条带

目的蛋白的条带存在多条带的情况:通过查阅蛋白数据库、文献排除翻译后修饰、蛋白亚型、剪切体等情况
1.样本原因
①样本降解
样本制备好进行分装,减少反复冻融;添加蛋白酶抑制剂;使用新鲜样本
②样本上样量过多
减少蛋白上样量
③样本未充分变性
制样时需添加足量的还原剂DTT或者BME,煮沸5-10分钟
2.抗体原因
①一抗非特异性结合
降低一抗浓度;一抗稀释液推荐使用5%脱脂牛奶;减少抗体孵育时间;选择高质量的单克隆抗体
②二抗非特异结合
可以通过不加一抗,只孵二抗的阴性对照判断二抗非特异性结合;降低二抗浓度;二抗稀释液推荐使用5%脱脂牛奶;减少抗体孵育时间;选择高质量的二抗
3.实验操作
①封闭不足
更换封闭液;提高封闭浓度;延长封闭时间
②洗涤不足
推荐TBST中至少添加0.1%吐温20,增加洗涤的时间和次数;如果背景全黑,建议增加TBST中的NaCl浓度至500mM
③曝光过度
减少曝光时间
④其他
实验过程中使用到的各种缓冲液建议使用双蒸水来配置;抗体孵育过程中不能使膜变干;在操作和转移膜的过程中,应当使用专门的平头镊子轻拿轻放,避免皱褶和痕迹;转膜过程中的滤纸不要回收利用。
三.条带大小不正确

1.预染蛋白Marker指示不准确
预染蛋白分子量不同的缓冲条件下电泳时迁移特性可能会发生某些变化,可能导致一些偏差,如果需要精准定位蛋白分子量,可以使用非预染的蛋白Marker
2.细胞传代次数过多
复苏低代数的细胞进行实验
3.不同种属的细胞、组织本身存在差异
应从过表达、敲除/敲减结果去判断是否为目的条带
4.蛋白修饰
不同的蛋白修饰所呈现出来的分子量是不同的,即使都是某种修饰,也有高低程度之分,例如高度糖基化和低度糖基化;应查阅相关文献或者通过切胶质谱的方式来判断具体修饰方式
5.多聚体
使蛋白充分变性,添加足量的还原剂及煮沸蛋白
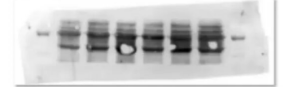
四.深背景出现白色条带

原因分析: 上样量过多,一抗二抗浓度过高
解决方案: 建议降低蛋白上样量;降低抗体浓度
五.电泳时溴酚蓝条带出现弯曲倾斜
原因分析
1.制胶玻璃板存在损坏缺口。
2.电泳槽装配存在问题,导致内槽漏液。
3.凝胶底部有气泡阻碍,导致电场分布不均。
解决方法
1.每次制胶前检查玻璃边缘有无崩口。
2.内槽灌注缓冲液后,观察液面是否下降。
3.外槽加满缓冲液,并用枪头去除凝胶底部的残留气泡。

六.微笑条带

原因解析
1.凝胶凝固不均,形成密度差异,影响蛋白迁移速率。
2.电压太高导致蛋白迁移速度快于两边。
3.电泳缓冲液重复使用导致缓冲能力下降。
解决方法
1.确保制胶架水平,给凝胶充足凝固时间(室温1小时或37℃加速聚合)。
2.可适当降低电泳电压,浓缩胶用80-90V,分离胶用100-120V。3.使用新鲜电泳缓冲液,也可采取冰浴电泳。
七.皱眉条带
![]()
原因解析
1.样品中含不溶性颗粒或高浓度盐,导致其在孔中沉淀,影响电泳迁移;上样量过大使样品孔中蛋白质浓度过高,中间部分迁移受阻。
2.电压波动、电流不稳定等因素影响蛋白质迁移。
解决方法
1.蛋白样品进行离心,避免吸取不溶性杂质;稀释样品,减少蛋白上样量。
2.适当降低电泳电压、减少电流,或使用恒流电源确保电流稳定。
八."哑铃"状条带(两头大中间小)

原因解析
1.凝胶未配置好。如凝胶浓度不均一、凝胶中有气泡或残胶等都可能导致蛋白质在电泳过程中的迁移速度不一致,形成哑铃型条带。
2.样品问题。样品中含有过多杂质,这些杂质在电泳过程中可能沉积在泳道中间,将蛋白质挤压到两边,形成哑铃型条带。
3.加样操作问题。加样时样本体积过少,未平铺铺满凝胶点样孔底部。
解决方法
1.优化凝胶配制,确保凝胶配制过程中使用干净的试剂和容器,充分混匀制胶液,避免气泡和杂质的产生。上样前吹打加样孔,去除残胶。
2.对样品进行适当的离心处理,如样品过于黏稠可以进行超声处理,以去除杂质。选择适当的上样体积,确保点样孔底部均匀
九.波浪状条带

原因解析
1.电泳时电压过高,产热多,或者电泳速度过快,凝胶变形。
2.转膜过程产热过多,条带扭曲。
3.制胶时凝胶凝固不均一。
4.转膜时夹的过紧,导致凝胶变形。
解决方法
1.适当降低电泳电压、减少电流,或使用恒流电源确保电流稳定。
2.使用新鲜电泳缓冲液,也可采取冰浴电泳。
3.优化凝胶配制,充分混匀制胶液,避免气泡和杂质的产生。
4.转膜夹别夹太紧。
十.条带中间出现空泡
原因解析
转膜时“滤纸-PVDF膜-蛋白凝胶-滤纸”中存在气泡,电流无法将蛋白分子转移至PVDF膜导致。
解决方法
1.组装转膜“三明治”时,尽量使转膜缓冲液没过凝胶。
2.在铺放滤纸和PVDF膜时,将滤纸或PVDF膜完全浸湿,从一侧轻轻放下,用刮板或滚轮彻底排出气泡。
十一.条带连在一起

1.蛋白上样量过大。解决方法
2.蛋白样品盐离子浓度过高。
3.抗体浓度过高,孵育时间过久,曝光时间长。
解决方法:
1.降低蛋白上样量。
2.蛋白纯化、透析处理,减少样品中的盐离子浓度。
3.降低抗体浓度,缩短孵育和曝光时间。
十二.条带拖尾
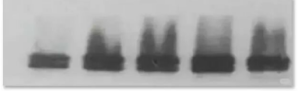
原因解析
2.蛋白出现轻微降解。
3.电泳液重复使用。解决方法
4.封闭不彻底,洗膜时间过短。
解决方法:
1.稀释蛋白样品,建议总蛋白20-50 μg/孔。
2.提取蛋白时在冰上操作,加入蛋白酶抑制剂,如样品粘稠建议超声处理。
3.配置新鲜电泳缓冲液。
4.延长封闭和洗膜时间。
十三.条带飘样

原因解析
1.转膜时夹的不够紧,凝胶与PVDF膜出现滑动或者接触不良。
2.转膜时电压或者电流不稳定或者放热过多。
3.PVDF膜老化或者损坏,导致蛋白转膜不稳定。
解决方法
1.避免使用质量不佳的转膜夹,建议使用3层滤纸。
2.更换稳定的电源,转膜期间更换冰袋,避免转膜过度放热。
3.保证PVDF膜没有褶皱损坏,并且彻底活化。
十四.条带皱缩不规则

原因解析
1.电泳电压过低,蛋白泳动速度过低出现弥散。
2.转膜时间长或者转膜电流大,放热过多导致凝胶变形。
3.PVDF膜的湿润不均匀、膜上存在污染物、膜过期、损坏等。
4.转膜滤纸多次使用,纸屑过多。
5.蛋白转膜液试剂配比错误或者包含杂质过多。
解决方法
1.使用新鲜的电泳缓冲液,根据蛋白分子量大小设置合适电压。
2.使用新鲜配制的转膜缓冲液,冰浴转膜。
3.转膜时保持全程低温,对于大分子量蛋白,转膜期间可更换冰袋。
4.使用品质有保证的PVDF膜以及配套的完好的转膜设备,避免转膜夹夹的过松或者过紧。
5.滤纸尽量不要多次使用,避免掉落杂质








 沪ICP备2022016794号-3
沪ICP备2022016794号-3